
A highly sensitive signal-on biosensor for microRNA 142-3p based on the quenching of Ru(bpy)32+–TPA electrochemiluminescence by carbon dots and duplex specific nuclease-assisted target recycling amplification[J]. Chemical Communications, 2020, 56.
电化学发光(ECL)是电极表面发生电化学反应时产生的一种化学发光现象。Ru(Bpy)32+(bpy=2,2’-联吡啶)三丙胺(TPA)体系具有电化学发光效率高、光化学稳定性好、与水介质中被分析物相容性好等优点,是目前应用最广泛的电化学发光体系之一。大多数基于Ru(Bpy)32+的电化学发光生物传感器通过调节电化学发光指示剂来实现目标的定量。例如,我们的团队利用二茂铁作为猝灭化合物来抑制Ru@SiO2纳米颗粒的ECL发射,并开发了一种灵敏的腺苷ECL生物传感器。基于多壁碳纳米管(MWNTs)对Ru(Bpy)32+-TPA体系ECL发射的猝灭性能,研究了多壁碳纳米管(MWNTs)对Ru(Bpy)32+-TPA体系ECL发射的猝灭性能,发现MWNTs表面的含氧基团和本征电子性质是抑制ECL的关键因素。报道了氧化石墨烯(GO)能猝灭Ru(Bpy)32+-TPA体系的电致发光,抑制电致发光的主要原因是GO的含氧基团和较差的导电性。作为一种生物相容性、无毒、水溶性和环境友好的纳米材料,碳点(CdS)由于其独特的发光性能和优异的催化性能,已被应用于构建众多的生物传感器。化学氧化法合成的CdS富含含氧官能团,初步研究表明CdS还能猝灭R Ru(Bpy)32+-TPA体系的ECL。
MicroRNA(MiRNA)的异常表达与心血管疾病、神经系统疾病及多种癌症有关。MiRNA 142-3p已被证实与宫颈癌、大肠癌、食管鳞癌等密切相关。因此,对其进行定量检测具有重要的临床意义。实时PCR、Northern印迹、芯片分析、荧光和电化学等多种有效的检测miRNA的方法已经发展起来。由于miRNA的痕量,需要采用信号放大策略来满足准确的检测要求。为了提高检测方法的灵敏度,引入了滚环扩增(RCA)、杂交链式反应(HCR)、核酸外切酶辅助循环扩增等一系列信号放大策略。双链特异性核酸酶(DSN)以其高特异性切割双链DNA或DNA-RNA双链而闻名,它不能作用于单链DNA和单链或双链RNA,已被广泛用于实现靶循环和信号放大。
本研究首次用碳点(Cd)猝灭Ru(Bpy)32+-三丙胺(TPA)体系的电化学发光(ECL)。此外,将这一现象与双链特异性核酸酶辅助的靶循环扩增相结合,开发了一种高灵敏度的微RNA ECL生物传感器。
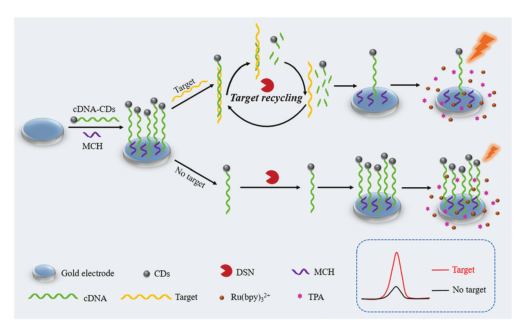
流程图:基于Ru(Bpy)32+-TPA ECL对Ru(Bpy)32+-TPA ECL的碳点猝灭和双链特异性核酸酶辅助的靶循环扩增,构建了miRNA142-3P信号导通生物传感器。